血管瘤和脉管畸形分类
1982 年, John B.Mulliken 首次提出基于血管内皮细胞生物学特性的分类法, 将传统的血管瘤(Vascular anomalies)重新分为血管瘤(Hemangioma)和脉管畸形(Vascular malformation)。这一分类观点被广泛认同,ISSVA 于2018 年对该分类系统再次修订。本文就此次修订的主要变动进行介绍,并附上最新的分类系统。
聊城市人民医院口腔科刘建林
婴幼儿血管瘤的分型包括单发型、多发型、节段型、中间型。其临床分类可分为浅表性、深在性、混合性(即浅表性+深在性)、网状性/顿挫性/微增生性和其他。
婴幼儿血管瘤还可合并其他病变, 如PHACE综合征(表现为:后颅凹畸形、血管瘤、动脉病变、心血管病变、眼病变、胸骨裂和/或脐上裂缝等),LUMAR(SACRAL/ PELVIS)综合征(表现为:下半躯体血管瘤,泌尿生殖系统病变,溃疡,脊髓病变,骨畸形,肛门直肠畸形,动脉病变,肾脏病变等)。
暂未归类的脉管性病变* 包括:肌间血管瘤**、角化性血管瘤、窦状血管瘤、肢端动静脉瘤、多发性淋巴管内皮瘤病合并血小板减少/皮肤内脏血管瘤病合并血小板减少(MLT/CAT)、PTEN(型)软组织错构瘤/软组织"血管瘤病"(PHOST)和纤维脂肪性血管性病变(FAVA)等。其中,某些疾病合并血小板减少和/或消耗性凝血功能障碍;肌间血管瘤不同于普通IH。
虽然, 在脉管畸形领域多个学科都有各自的分类方案, 但鉴于ISSVA 分类具有前瞻性和实用性,已经在脉管畸形领域长期、广泛使用,故本学组采用ISSVA 分类(2018)方案为本指南分类方案。
血管源性肿瘤的诊断和治疗
1 婴幼儿血管瘤
1.1临床表现
婴儿血管瘤是指由胚胎期间的血管组织增生而形成的,以血管内皮细胞异常增生为特点,发生在皮肤和软组织的良性肿瘤。最早期的皮损表现为充血性、擦伤样或毛细血管扩张性斑片。出生后6 个月为早期增殖期,瘤体迅速增殖,明显隆起皮肤表面,形成草莓样斑块或肿瘤, 大小可达最终面积的80%。之后增殖变缓,6~9 个月为晚期增殖期。节段型血管瘤和深在型血管瘤增殖期可持续至9~12 个月,少数患儿增殖期甚至可持续至出生后24 个月。有一小部分瘤体表现为微小增殖或不增殖,主要位于下肢,这部分瘤体应注意与毛细血管畸形区别。90%的患儿在4 岁时瘤体完全消退,瘤体累及越深,消退时间越晚。未经治疗的瘤体消退完成后有25%~69%的患儿残存皮肤及皮下组织退行性改变, 包括瘢痕、萎缩、色素减退、毛细血管扩张和皮肤松弛等。
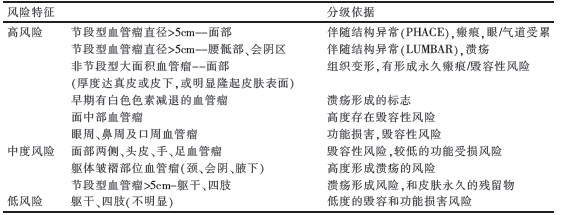
根据相关文献, 建议将血管瘤分为3 个风险等级(表2)。
表2 血管瘤的风险等级及分级依据

1.2诊断及鉴别诊断
婴儿血管瘤依病史、临床和影像学可确诊。浅表型婴儿血管瘤早期应与微静脉畸形区别;深在型婴儿血管瘤应与脉管畸形(静脉畸形、动静脉畸形等)区别(表3)。部分婴儿血管瘤需与先天性血管瘤、卡波西型血管内皮瘤等鉴别,通过瘤体生长及消退特征、临床表现及病理检查等可鉴别。深在型血管瘤还应与钙化上皮瘤、皮样囊肿、平滑肌肉瘤、淋巴瘤等鉴别。
表3 婴儿血管瘤与脉管畸形的鉴别诊断


1.3辅助检查
90%以上的患儿局部B 超检查即可了解瘤体的范围及血供情况,少数位于头皮、骶尾部及重要器官周围的瘤体,需行MRI 检查,以了解是否累及周围组织器官及侵及的程度。位于眼周、耳周等部位的瘤体,需眼科、耳鼻喉科等相关科室会诊,评估眼、耳等器官功能是否受损。巨大或多发的肝脏血管瘤、PHACES 综合征、骶尾部的血管瘤,需行超声心动图检查,以了解有无心功能不全、心脏或主动脉结构异常等。肝脏多发血管瘤, 需行凝血功能及血小板检查,了解有无DIC。全身多发血管瘤,需行甲状腺功能检查,了解有无甲状腺功能低下。
1.4治疗
1.4.1 治疗方法及适应证
婴儿血管瘤主要以局部外用和系统用药为主,辅以激光或局部注射等, 目的是抑制血管内皮细胞增生、促进瘤体消退和减少瘤体残留。①高风险血管瘤:尽早治疗。一线治疗为口服普萘洛尔,若有禁忌证,则系统使用糖皮质激素。②中等风险血管瘤:尽早治疗。早期而菲薄的病灶可给予外用β 受体阻滞剂,也可加用脉冲染料激光;治疗过程中,若不能控制瘤体生长,则遵循高风险血管瘤治疗方案。③低风险血管瘤:如很稳定,可随诊观察,或尝试使用外用药物;如瘤体生长迅速,则遵循中等风险血管瘤治疗方案。④消退期和消退完成期血管瘤的进一步治疗,以唇部血管瘤的整形治疗为例, 最佳年龄是3~4岁,因为之后血管瘤自发改善不再明显。如果推迟治疗,则可能对患儿心理或其他功能造成影响。
1.4.2 治疗方法的选择
1.4.2.1 局部外用药物
适用于浅表型婴幼儿血管瘤的常用药物:①β受体阻滞剂类,如普萘洛尔软膏、噻吗洛尔乳膏、噻吗洛尔滴眼液、卡替洛尔滴眼液等。外涂于瘤体表面,每天2~4 次,持续用药3~6 个月或至瘤体颜色完全消退, 通常用药第2~3 个月时疗效最为明显。除个别报道有变态反应性接触性皮炎外, 还可能有发红、脱屑等局部不良反应。②5%咪喹莫特:隔日夜间睡前薄层外涂于瘤体表面,次日洗去,疗程16 周。常见皮肤反应有红斑、糜烂、溃疡结痂等,发生不良反应时需及时停药,等待皮肤恢复后方可继续用药。由于该药物易引起皮肤强烈的免疫反应, 导致后期皮肤质地改变甚至瘢痕形成,故建议慎用,包括有外用β 受体阻滞剂禁忌证的患儿。
1.4.2.2 局部治疗
①糖皮质激素注射:主要适用于早期、局限性、深在或明显增厚凸起的血管瘤, 治疗终点为病灶体积缩小,甚至接近平坦。在眼周甚至更远区域,偶有报道可能因注射物逆流导致眼动脉及其他动脉栓塞、缺血,从而导致严重并发症。
②博来霉素、平阳霉素及其他抗肿瘤药物注射:用于口服或局部注射糖皮质激素效果不佳时, 为防止偶发的过敏, 建议在注射过程中保持静脉补液通畅。过度治疗可晚期诱发注射区域发育迟缓或障碍。
③局部脉冲染料激光:通常为585 nm 或595 nm脉冲染料激光, 常用于浅表型婴儿血管瘤增殖期抑制瘤体增殖,血管瘤溃疡、消退期后减轻血管瘤的颜色或毛细血管扩张性红斑。该治疗方案并无病灶选择性,对深部病灶无法抑制其生长,以不形成新的皮肤损伤为前提。
1.4.2.3 系统治疗
①普萘洛尔:建议剂量为1.5~2 mg/Kg·d,分2次服用。校正年龄<3>3 个月患儿给予2 mg/Kg·d,分2 次服用。使用本药物治疗时要注意适应证,用药前应对患儿进行全面体检,包括心肌酶、血糖、肝肾功能、心电图、心脏彩超、甲状腺功能等。校正年龄2个月以上的患儿治疗可在门诊进行, 由家长对患儿服药后情况进行监测。校正年龄<2 个月的患儿或体重<2 Kg 的低体重儿, 最初服药3 天建议入院严密监测,治疗起始剂量为每天1 mg/Kg,分2 次口服。首次服药后观察患儿有无肢端湿冷、精神萎靡、呼吸困难和明显烦躁等现象。如患儿能够耐受,首次服药12 h 后继续给药,剂量仍为0.5 mg/Kg。如患儿仍然无明显异常,第2 天增量至每天1.5 mg/Kg,分2 次口服,并密切观察。如无异常反应,第3 天增量至每天2 mg/Kg,分2 次口服,后续治疗以此剂量维持。服药期间定期复诊,服药前3 个月应4 周复诊一次,3 个月后可8 周复诊一次,10 个月后可12 周复诊一次。每次复诊应复查生化、心电图、心脏彩超及局部B 超,以评估不良反应及疗效,若出现心肌损害、心功能受损、喘息、低血糖等情况,应对症治疗或由相应科室会诊,在此期间,普萘洛尔剂量应减半,不良反应严重时需停用。口服普萘洛尔瘤治疗婴儿血管瘤无确切停药年龄限制, 瘤体基本消退(临床及B超结果证实)时可考虑停药。大多数患儿服药后瘤体不能达到完全消退, 在瘤体达到最大消退程度超过3 个月且患儿年龄超过1 周岁时, 也可建议其缓慢停药,因为可能会出现停药后复发现象。停药时患儿年龄超过17 月龄以上,则复发风险显著降低。
②糖皮质激素:口服泼尼松3~5 mg/Kg(总量不超过50 mg),隔日早晨1 次顿服,共服药8 周;第9周减量1/2;第10 周,每次服药10 mg;第11 周,每次服药5 mg;第12 周停服,完成1 个疗程。如需继续,可间隔4~6 周后重复上述疗程。该治疗现可用于具有全身用药适应证而不适合于普萘洛尔治疗的病例。用药期间可能有身高、体重和血压等的暂时性影响,应密切监测,服药期间应停止疫苗接种,直至停药后6 周以上。
2 先天性血管瘤
2.1 临床表现
先天性血管瘤(Congenital hemangioma,CH)是一类特殊类型的良性血管瘤。不同于婴幼儿血管瘤,先天性血管瘤在母体子宫内发生发展, 患儿在出生时即有明显病灶。先天性血管瘤区别于婴幼儿血管瘤的另一个特点是其缺乏出生后的增殖期。目前,ISSVA 分类系统中,将已知的先天性血管瘤分3 类:快速消退型CH (Rapidly Involuting Congenital Hemangioma, RICH), 不消退型CH (Non-Involuting Congenital Hemangioma, NICH) 和部分消退型CH(Partially Involuting Congenital Hemangioma, PICH)。不同于婴幼儿血管瘤的女性好发倾向, 先天性血管瘤男女发病率接近1∶1。病灶好发于头面部和肢体,多为单发,偶见多发。绝大多数先天性血管瘤病灶累及皮肤软组织, 完全位于皮下而不累及皮肤者极罕见,亦有发生于肝脏的先天性血管瘤(RICH)。病灶形态多为隆起或斑块状, 边界清楚, 紫红色或蓝紫色,表面有粗细不等的毛细血管分布,周围可见白色的晕环,病灶周围可见放射状分布的浅表扩张静脉。病灶皮温常高于周围皮肤,有时可触及搏动。不同类型的先天性血管瘤出生后呈现各自特征性的临床表现。RICH 在出生后不久即开始快速消退,大约6~14个月时病灶完全消退,残留松弛、菲薄的皮肤,皮下脂肪缺失。在RICH 快速消退过程中可出现并发症,如出血、溃疡等。极少数巨大RICH 可因病灶内动静脉瘘造成的动静脉分流而造成心功能衰竭。RICH还可伴发凝血功能障碍,表现为血小板降低、纤维蛋白原降低、D-二聚体升高。NICH 在出生时往往与RICH 难以鉴别,出生后其最显著的特点是病灶随身体等比例生长,既不增殖也不消退。病灶表面皮肤可出现部分苍白, 表面毛细血管往往较RICH 更为粗大,病灶周围白色晕环较RICH 更常见。PICH 在出生后先经历类似RICH 样的快速消退期, 然而在病灶尚未完全消退时消退中止。消退中止后的残留病灶与NICH 难以区分。因此,有研究认为PICH 的存在是RICH 可转化为NICH 的可能证据。目前,三种先天性血管瘤是否是同一起源尚无定论。
2.2 诊断与鉴别诊断
根据典型临床表现和出生后生长行为可诊断大多数先天性血管瘤。依据各自特征性的临床表现不难区分出3 种先天性血管瘤。先天性血管瘤需与婴幼儿血管瘤相鉴别, 先天性血管瘤病灶与婴幼儿血管瘤的前驱病灶在外观上并不相同。在出生时,婴幼儿血管瘤的前驱病灶多表现为皮肤白斑、红点或片状的毛细血管, 而非先天性血管瘤那样显著增大的瘤体。出生后,先天性血管瘤与婴幼儿血管瘤的临床表现完全不同。病理上,先天性血管瘤与婴幼儿血管瘤的小叶结构特点不同。此外,GLUT-1 是鉴别先天性血管瘤与婴幼儿血管瘤的重要标志, 婴幼儿血管瘤小叶内皮细胞均阳性表达, 而先天性血管瘤中为阴性。先天性血管瘤还需与少见的中间性血管瘤(如卡波西型血管内皮瘤)鉴别。卡波西型血管内皮瘤在少数情况下可表现为先天性病灶。所不同的是,在出生后, 多数卡波西型血管内皮瘤呈现进展性临床病程,病灶呈浸润性生长,质地较硬。需要注意的是,以往常将RICH 伴发的凝血功能异常与卡波西型血管内皮瘤和丛状血管内皮瘤伴发的卡梅现象混淆。事实上,RICH 所伴发的凝血功能异常极为少见,而卡梅现象在卡波西型血管内皮瘤中并不少见。RICH伴发的凝血功能异常血小板降低的程度与凝血功能紊乱的严重程度均明显轻于卡梅现象, 且随着瘤体的快速消退,症状逐步缓解;与之相反,卡梅现象症状随卡波西型血管内皮瘤病情进展迅速加重。先天性血管瘤还需与脉管畸形相鉴别。NICH 与动静脉畸形的临床表现有相似性,两者均表现为高流量,病灶皮温均明显增高,NICH 的等比例生长方式也与Ⅰ期动静脉畸形相似。早期文献中有将NICH 诊断为AVM 的先例。然而,动静脉畸形病灶主要由包含动静脉瘘的畸形血管团构成; 而NICH 病灶由大量增殖的内皮细胞和周细胞构成, 是真性的软组织肿瘤,并非真正的动静脉瘘,影像学检查可协助鉴别。先天性血管瘤更需与其他少见的先天性软组织肿瘤鉴别,特别是恶性肿瘤(如软组织肉瘤等),当遇到诊断及鉴别诊断困难时,病理活检是十分重要的手段。
2.3 辅助检查
多普勒超声是重要的辅助检查手段。产前超声检查可最早可在妊娠12 周时检测到先天性血管瘤。然而,受病灶大小、部位、检查者水平和经验限制,并非所有先天性血管瘤均可在子宫内被检测到。出生后超声检查是一种简单、有效的方法。病灶多表现为边界清楚的软组织团块,具有丰富的动静脉血流,可见病灶内扩张的管道样结构。MRI 和CT 可用于进一步检查。MRI 可清楚显示病灶大小、结构、范围以及与周围组织的关系。病灶特点是边界清楚, 呈现T1 低信号,T2 高信号,均匀强化,病灶内的流空影提示高血流量特点。此外,在先天性血管瘤病灶内可发现动脉瘤、血栓及钙化,这在婴幼儿血管瘤中极罕见,有助于鉴别诊断。当需要与动静脉畸形鉴别时,CTA 或DSA 可明确病灶有无动静脉瘘。
2.4 治疗
RICH 具有快速消退的特点, 不需要提前治疗干预。治疗主要针对巨大RICH 本身所致或快速消退时所伴发的并发症。巨大RICH 病灶内动静脉瘘造成动静脉分流诱发心功能衰竭, 或出现凝血功能异常时,可先采用药物对症治疗,当药物治疗无法缓解症状, 且症状严重甚至威胁生命时, 供血动脉栓塞, 甚至手术切除病灶是需要考虑的治疗手段。RICH 在消退过程中出现病灶表面溃疡或出血可先采用非手术治疗,压迫止血,保护和处理创面,随着病灶的消退, 症状多可自行缓解, 溃疡自行结痂愈合。包括手术和介入为主的外科治疗在非手术治疗无效或症状进行性加重时方考虑介入。RICH 消退后残留松弛的皮肤和周围扩张静脉,皮下脂肪缺失。此时,治疗的主要目的是改善外观。可采用的方法有手术切除多余皮肤、局部脂肪充填、激光改善肤质、消除扩张静脉。NICH 和PICH 并非都有治疗指征。治疗指征主要包括当病灶位于特殊部位影响功能(如上睑病灶遮挡视野),或病灶影响外观,造成患儿及其家长的心理障碍。手术切除是有效的治疗方式,多数病灶可一期完整切除,术后复发少见。
3血管内皮瘤
3.1 种类
血管内皮瘤指血管内皮来源的交界性肿瘤,包括卡波西型血管内皮瘤(Kaposiform hemangioendothelioma,KHE)、丛状血管瘤(Tufted angioma,TA)和其他少见血管内皮瘤(混合性血管内皮瘤、网状血管内皮瘤、多形性血管内皮瘤、淋巴管内乳头状血管内皮瘤等)。这一类肿瘤生物学行为介于良、恶性之间,在局部呈侵袭性生长。
3.2 临床表现
3.2.1 KHE 与TA
KHE 属于交界性血管肿瘤,无远处转移,但具有局部侵袭性,可累及体表多个部位或深部脏器。新生儿中发病率约0.7/1 000 万, 在血管肿瘤中约占2%。绝大多数KHE 病例在1 岁之内发病(90%),其中1 月龄内发病占60%。体表KHE 病灶通常表现为皮肤或皮下坚韧肿物,外观呈紫红色结节或斑块,色泽常深浅不一, 边缘因淤斑或毛细血管扩张而界限不清。自然病程中,婴儿期发病的KHE 常有快速增长期,之后虽有不同程度的缓慢缩小,但不能完全消退。残留病灶性状不一,常呈葡萄酒色斑样改变,皮肤表面散布丘疹及毛细血管扩张, 伴有肿胀和纤维化的质地改变。KHE 和TA 可引起卡梅现象(Kasabach-Merritt phenomenon,KMP), 这是在脉管性疾病基础上伴发血小板减少、微血管溶血性贫血和消耗性凝血功能障碍的一类临床表现, 其病程凶险,患者往往因凝血功能紊乱、败血症以及重要器官的损害而预后不佳。胸腹腔、纵膈、腹膜后的KHE 病灶常累及重要脏器, 血流量较高而极易引发KMP,且发病隐匿,病程凶险,常因呼吸窘迫、腹部膨隆、肌张力减退或便血而就诊。此外,累及肌肉的KHE 病灶同样因为血流丰富而比单纯的皮肤、骨骼病灶更易引发KMP。但就单个病例而言,KHE 病程难以预测, 创伤、感染甚至血制品输注都可能触发瘤体增大、紫癜和疼痛,进而伴发KMP。TA 同样好发于婴幼儿,半数以上在婴儿期发病,近70%在10 岁前发病,且发病越早则自然消退的趋势越明显。增生期通常为5 个月至10 年,此后保持稳定,自发消退仅占10%。TA 的临床症状与KHE 的皮肤病灶类似,但浸润深度浅,也无内脏的累及。因此,体积较大、累及至肌肉的TA 可能引发KM 现象, 病灶可因红肿热痛而被误诊为局部炎症。
3.2.2 Kasabach -Merritt 现象(Kasabach –Merritt phenomenon,KMP)
KMP 是KHE 和TA 特有的重症临床表现,是在脉管性疾病基础上伴发血小板减少、微血管溶血性贫血和消耗性凝血功能障碍的一类临床表现, 其病程凶险,患者往往因凝血功能紊乱、败血症以及重要器官的损害而预后不佳。KMP 的自然病程始于KHE/TA 病灶对血小板的捕获, 外周血中血小板减少,病灶微血管内血小板聚集形成血栓,致使红细胞流经狭窄管腔时被压碎、割裂发生血管内溶血。活化的血小板释放促血管新生介质, 且纤溶系统的相应亢进可造成瘤内出血, 病灶因此快速增大并引起新一轮的凝血物质消耗,最终诱发DIC,重症患儿常因颅内、消化道出血或重要脏器功能衰竭而死亡。
3.3辅助检查
影像学检查可辅助诊断及鉴别诊断。彩色多普勒超声可检测病灶内血流量, 与其他低流量或高流量脉管畸形相鉴别。增强CT 及MRI 对KHE/TA 诊断亦有价值,CT 平扫表现为均匀或不均匀的低密度灶, 增强呈明显强化。MRI 有利于明确病灶范围,MRI 中T1W1 序列呈等、低信号,T2W1 序列呈等高信号,增强呈不均匀显著强化。实验室检查用于监测KMP 的发生和进展,血小板通常低于50×109 /L。诱发DIC 时, 纤维蛋白原明显降低,PT 和APTT 轻度延长,纤维蛋白降解产物(FDP)或D-二聚体增高,同时有一定程度的微血管病性溶血性贫血。
3.4诊断
特征性的临床表现结合辅助检查可临床诊断部分KHE 与TA 病例。然而,由于交界性肿瘤的生物学性质, 血管内皮瘤的确诊需要严格的组织病理学诊断。KHE 病灶中可见大量形状各异、边界模糊的结节向周围浸润, 边缘伴随着恶性肿瘤中常见的间质反应,结缔组织呈致密的玻璃样变。结节内部形态结合了婴幼儿血管瘤和卡波西肉瘤的特点, 既有成团的梭形内皮细胞,也有高度迂曲、缠绕的微血管,还有大量发育不良的狭缝状管腔,其中充满红细胞,类似卡波西肉瘤。2/3 的病灶中可见畸形的薄壁淋巴管包绕结节并向周围延伸, 少数病灶旁中甚至可见大量的淋巴管增殖,类似淋巴管畸形。此外,病灶中还散布着由圆形透明细胞、含铁血黄素和微小空泡组成的肾小球样结构, 其中可见血小板聚集形成的血栓。结节中内皮细胞表达CD31、CD34、VEGFR-3、D2-40、PROX-1 和FLI1,不表达婴幼儿血管瘤相关抗原表达GLUT-1 和LeY。TA 病灶中的微血管被紧密压缩成小叶状,以炮弹形态分布于真皮网状层,较少浸润至皮下,分布不如KHE 的结节集中,体积也较小。真皮深层的小叶较浅层更大, 并常融合成簇。由于成管不完全,小叶中多种形状(圆形、椭圆和梭形)的内皮细胞以及大量周细胞聚集成团,类似婴幼儿血管瘤。其周围分布的薄壁新月形血管腔和膨大的淋巴管腔也是TA 的特征之一。此外,KHE 病灶中央呈卡波西肉瘤样的微血管在D2-40 染色中为阳性,周围扩张的淋巴管为阴性;TA 则相反,周围扩张的淋巴管在该染色中为阳性, 中央呈炮弹样分布的微血管小叶为阴性。其他少见血管内皮瘤亦有各自特征性的病理表现。
3.5治疗
3.5.1 KHE 与TA
KHE 和TA 的治疗方法包括手术切除、介入栓塞,以及全身用药和血制品等3 类。根据病情进展的轻重缓急,治疗策略大体上可分为三类:①无临床症状,也无增大趋势的体表病灶可密切随访;②有临床症状或增大趋势的体表病灶,以及所有内脏病灶,均需积极治疗。由于可完整切除且不遗留功能毁损的病灶极少见, 因此全身用药应是第一选择;③伴有KMP 的病灶应在积极治疗肿瘤的基础上,酌情应用抗凝药物和血制品,以改善凝血功能。
手术切除通常是肿瘤的首选治疗, 但KHE/TA病灶界限不清,常累及重要血管、神经甚至脏器,极大地增加了手术风险和功能毁损可能。因此,仅少数局限、表浅的病灶可手术完整切除。
介入栓塞可在DSA 辅助下利用药物或材料封堵KHE/TA 的主要滋养血管,暂时缩小病灶,改善凝血功能,为进一步的手术或药物治疗创造条件。由于存在肢体、器官缺血梗死的风险,不推荐在凝血功能恶化的危重病例之外作为首选。
全身用药是目前KHE/TA 治疗的首选, 但众多用药方案的循证医学证据等级普遍较低。近期的大样本临床试验表明, 雷帕霉素的有效性和安全性足以作为一线药物, 且联合糖皮质激素后可显著改善KMP。尽管雷帕霉素与常用一线药物长春新碱的临床对照试验尚未结束,但两者共同作为一线方案,互为备选,无疑是目前较为合理的治疗策略。普萘洛尔已被证实对KMP 效果不佳,不建议单独使用。
雷帕霉素的推荐剂量为0.8 mg/m2(体表面积),每日2 次口服,每月监测血药浓度(10~15 ng/mL),伴发KMP 时联合应用泼尼松龙2 mg/Kg·d 口服或甲强龙1.6 mg/Kg·d 静脉滴注,泼尼松龙、甲强龙和地塞米松之间可按20∶16∶3 的比例换算。雷帕霉素的常见副作用为口腔溃疡、消化、血液和代谢功能的紊乱,通常在减量和停药后可逐步恢复。由于KHE 病例中以婴幼儿患者居多, 在用药过程中务必严格控制血药浓度, 并预防性使用抗生素以预防严重凶险性感染, 如应用复方新诺明以预防卡氏肺孢子菌肺炎等。避免和减轻副作用的关键在于设定合理的治疗目的,即有效控制临床症状,缩小病灶而不是彻底消退。作为非恶性肿瘤,KHE/TA 患儿的带瘤生存是常态,尤其是累及肌肉伴发KMP 的病灶在治疗后期常发生致密的纤维化。雷帕霉素连续应用1 年的病例中,后半年的瘤体消退进度明显慢于前半年,因此一旦病灶大小趋于稳定, 症状也没有进一步改善的趋势时,应考虑逐步减量至停药,疗程一般不超过2 年。此外,糖皮质激素在当凝血功能和血小板计数稳定后也应该逐渐减量至停药,通常为6~9周。
长春新碱推荐剂量为0.05 mg/Kg, 每周1 次静脉滴注, 伴发KMP 时联合泼尼松龙2 mg/Kg·d 口服,可在1~3 周内显著改善症状。长春新碱的具体疗程同样取决于症状改善、瘤体缩小与副作用耐受的程度,通常为20~24 周。常见副作用为腹痛、深腱反射缺失与易怒。
KMP 的对症治疗包括抗凝药物和血制品输注。抗凝药物应用于血小板显著减少的病例具有一定争议, 但血小板的聚集活化和释放促血管新生介质是KMP 起始和加重的主因,因此抗血小板药物是对症治疗的重要手段,能够缩短抗肿瘤治疗的疗程。大量针对KMP 的临床研究已证实抗血小板治疗对无活动性出血病例的安全性,并不会增加出血风险,且联合用药效果优于单药治疗。常用方案为阿司匹林和噻氯匹定,其中阿司匹林(2~3 d)抑制环氧酶活性以阻止血小板聚集,噻氯匹定(4~7 d)则可阻断ADP诱导的血小板聚集和血小板释放具有促血管新生作用的α 颗粒。
血制品输注包括血小板、红细胞、血浆、冷沉淀及纤维蛋白原。由于KMP 源于KHE/TA 病灶对血小板的捕获,而非血小板生成障碍,输注的血小板半寿期极短(1~24 h),并可促使瘤体增大、疼痛加重,因此输注血小板仅适用于有明显出血倾向或术前准备的病例。血红蛋白<80 g/L 的贫血患儿需输注红细胞悬液支持治疗。在纠正低纤维蛋白原血症(<1 g/L),尤其是合并活动性出血时, 补充经过病毒灭活的纤维蛋白原浓缩物应首先考虑,其次是冷沉淀输注,最后才考虑输注冰冻血浆, 因为通过血浆补充纤维蛋白原需要较大的用量。
3.5.2其他的少见血管内皮瘤
其他血管内皮瘤治疗相对较棘手,发生率较低,目前尚无治疗共识, 手术治疗被认为是唯一的根治方法。病灶较小者可通过手术完整切除,但手术复发率较高。如无明显增长或并发症,可选择观察随访。
脉管畸形的诊断和治疗
1 葡萄酒色斑
1.1 临床表现
葡萄酒色斑(port-wine stains,PWS)为最常见的毛细血管畸形(Capillary malformation,CM),又称鲜红斑痣,系先天性皮肤毛细血管扩张畸形,发病率为0.3%~0.5%,常在出生时出现,好发于头、面、颈部,也可累及四肢和躯干。表现为边缘清楚而不规则的红斑,压之褪色或不完全褪色。红斑颜色常随气温、情绪等因素变化。随着年龄的增长,病灶颜色逐渐加深、增厚,并出现结节样增生。部分严重的病变可伴有软组织和骨组织的增生,导致局部增大变形。可分为3 型:①粉红型,病变区平坦,呈浅粉红至红色,压之完全褪色;②紫红型:病变区平坦,呈浅紫红至深紫红,压之褪色或不完全褪色;③增厚型:病变增厚或有结节增生,压之不完全褪色或不褪色。
1.2诊断及鉴别诊断
单纯葡萄酒色斑根据病史、临床表现即可诊断。其组织病理学改变为真皮浅层毛细血管网扩张畸形,管壁仍为单层内皮细胞构成,表皮层及其周围组织正常。6 月龄内患儿需与婴儿血管瘤区别,早期两者都可表现为红斑, 但婴儿血管瘤有明确的增生过程,表现为可逐渐隆起且呈鲜红颗粒状,而葡萄酒色斑在幼儿期均呈平坦的红斑,病灶成比例增大。
发生在面部沿三叉神经分布的红斑, 需排除伴有Sturge-Weber 综合征(Sturge-Weber syndrome)。该综合征因病变侵及软脑膜, 有8%的患儿在婴儿期即出现惊厥,因可导致智力障碍和神经功能损害,需神经内科干预。此外,70%的该综合征患儿可出现脉络膜受累,其中30%出现青光眼,早期眼科干预可避免失明。发生在肢体的葡萄酒色斑还需与KT综合征(Klippel-Trénaunay syndrome,KTS)鉴别。KTS有三个临床特点:患肢大面积红斑、先天性静脉(淋巴管)畸形,以及骨和软组织增生肥大。另外,葡萄酒色斑还需要与毛细血管畸形-动静脉畸形(CMAVM)鉴别,后者为家族遗传性,可伴有全身多发的红斑,同时伴有深在的动静脉畸形病灶。
1.3辅助检查
葡萄酒色斑根据临床表现即可诊断。辅助检查主要用于鉴别综合征。Sturge-Weber 综合征需通过增强MRI 显示软脑膜的异常,还需眼压、眼底检查以筛查青光眼及脉络膜血管畸形。Klippel-Trénaunay综合征的影响主要是皮下组织的增生, 血管造影或MRI 有助于发现深部静脉畸形。CM-AVM 需要行CTA 三维血管成像、增强MRI 或血管造影来确诊AVM病灶。
1.4治疗
1.4.1激光治疗
利用血红蛋白吸收波段(532~1 064 nm)的脉冲激光治疗,是目前葡萄酒色斑的首选治疗方法。需根据患者个体和病情、局部反应等确定治疗参数,剂量过大将导致热损伤和瘢痕。重复治疗需间隔1~2 月。
1.4.1.1脉冲染料激光(Pulsed dye laser,PDL)
常用595 nm PDL,脉宽0.45~20 ms,需要根据光斑大小调节能量密度, 能量密度8~15 J/cm2;或585 nm PDL,脉宽0.45 ms,能量密度5~7 J/cm2;或585~600 nm 可调PDL,脉宽1.5 ms。治疗终点为皮肤即刻出现紫癜。通常使用动态冷却系统或冷风冷却系统来缓解疼痛,及避免热损伤等副作用。
1.4.1.2脉冲倍频Nd:YAG 激光
波长532 nm,脉宽5~30 ms,能量密度7~16 J/cm2。需根据治疗反应由小剂量开始逐步增加, 病灶颜色变暗呈灰紫色即为治疗终点。因532 nm 激光穿透较浅,黑色素吸收较多,色沉较其他波长激光治疗更为常见。
1.4.1.3长脉冲Nd:YAG 激光
波长1 064 nm, 脉宽1~60 ms, 能量密度30~100 J/cm2。因1 064 nm 激光穿透深,可用于增厚病变的治疗。该激光治疗时不易出现紫癜,但瘢痕发生率较其他激光治疗高。
1.4.1.4长脉冲翠绿宝石激光
波长755 nm,可用于增厚病灶,脉宽3~20 ms,治疗后色素沉着和瘢痕发生率较PDL 高。
1.4.2光动力治疗(Photodynamic therapy,PDT)
又称血管靶向光动力疗法(Vascular-target photodynamic therapy,V-PDT),是利用激光激发富集于畸形毛细血管内皮细胞中的光敏剂所产生的单线态氧,选择性地破坏畸形毛细血管网。该方法是继选择性光热作用治疗之后,另一靶向性强、疗效好、安全性佳,且无热损伤的治疗新技术。需根据患者个体和病情,制定个性化方案,主要参数包括光敏药物与剂量,激光参量与治疗量,以及治疗区规划等。
① 光敏药物:如血啉甲醚、血卟啉注射液等。按说明书进行皮试和静注,药量一般为2~5 mg/Kg,给药后即予照光。②治疗光源:首选连续激光,如532 nm半导体激光或全固态激光等,其激发光敏药物效率最高;其次可用高频脉冲激光(准连续激光),如511 nm或578 nm 铜蒸气激光等;再者可用630 nm 半导体激光,其穿透深度更深,但需注意深层正常血管网破坏的风险。用有扩束或光束整形装置的点状光纤,要求光斑大、边界清、光强分布均匀(光强差≤10%)。非激光光源有发光二极管(LED)和强光(IPL)等,LED 波长选择532 nm, 可作为光动力学治疗的光源,但需设定特定的光照距离以保证光源的稳定性,IPL 的激发作用和光束质量远不及激光, 无法经光纤传输,难以准确测量输出光量,使用时需检测照射区的光强度及均匀性。③照光剂量:功率密度即照射强度一般为80~100 mW/cm2。照光时间15~40 min,能量密度即照射光量为60~360 J/cm2。对特殊部位(如鼻翼、上唇、颏部、肢体等)应适当缩短照射时间,儿童患者需适当降低光照的功率密度。④用海姆泊芬后需避强光直射皮肤2~4 周,用血卟啉注射液后约需避光1~3 个月。⑤重复治疗需间隔至少2~4 个月。⑥麻醉:成人患者可局部使用表面麻醉剂或口服/肌注止痛剂,对于不能耐受疼痛的成人患者以及儿童患者可选择在全麻下进行, 减少治疗时的疼痛造成治疗部位的移动。
1.4.3非相干光治疗
强脉冲光治疗(Intense pulsed light,IPL),一般选用560 nm 或590 nm 的滤光片。需根据皮肤类型选择合适的能量密度和脉宽, 同样需避免热损伤导致的瘢痕和疼痛等副作用。
1.4.4手术治疗
对于非手术治疗无效的病例, 可采用手术治疗来清除病灶,或改善外观畸形。
1.4.4.1直接切除缝合
对于病灶较小的葡萄酒色斑, 经多次非手术治疗无效,或既往治疗已形成瘢痕,或病灶已增厚,可考虑一期手术切除后直接缝合。对于切除后拉拢缝合张力较大时,可适当向创缘两侧皮下广泛分离,或延长切口线,动员邻近皮肤组织量,达到一期缝合。
1.4.4.2局部皮瓣
对于按解剖亚单位分布的病灶, 可考虑采用局部皮瓣转位修复,经一期皮瓣转位修复成活后,再行皮瓣修整以达到较好的外观。在皮瓣组织量供区充足的情况下,尽可能一并切除亚单位内正常皮肤,以确保亚单位的完整重建,达到较好的美学效果。
1.4.4.3皮片移植
大面积葡萄酒色斑病灶切除后, 创面采用中厚皮片或全厚皮移植覆盖,是最传统的、简便易行的方法。该方法适用于面部大面积病灶无正常皮肤供区提供修复者、年龄较大的患者,以及自身条件无法耐受其他修复方法的患者。该方法最大的弊端就是术后皮片的颜色和质地无法与受区匹配,尤其是面部,存在明显的色差和面具样外观。
1.4.4.4组织扩张
面部皮肤质地具有特殊性, 其他部位的组织移植后无法重现面部组织的特性。采用组织扩张的方法获取病灶邻近的局部皮瓣或带蒂皮瓣,来修复病灶,能获得与原位组织最接近的修复效果。
1.4.4.5 预构扩张皮瓣
通过单纯组织扩张所获得的扩张皮瓣并不含有轴形血管, 皮瓣转移时将会受到随意皮瓣的血运规律的限制,转移和利用率都将受到很大影响。预构扩张皮瓣的核心是预先在扩张皮瓣内植入知名的血管束,构建轴型皮瓣,改善皮瓣血液供应,可减少皮瓣的坏死率。
1.4.4.6 正畸正颌手术
对于面部葡萄酒色斑合并的上下颌骨轮廓畸形,如骨骼肥大、咬牙合畸形,可联合正畸与正颌手术予以矫正。
2 静脉畸形
2.1 临床表现
静脉畸形(Venous malformation,VM),旧称海绵状血管瘤, 是静脉异常发育产生的静脉血管结构畸形, 病理表现为从毛细血管到腔穴不等的扩张血管腔窦,腔内壁衬以正常的扁平内皮细胞。内皮细胞下为一单层基底膜。血窦的管腔壁平滑肌稀少,外膜纤维变性。静脉畸形通常以单一静脉结构存在,也可与其他血管结构混合, 形成毛细血管静脉畸形或淋静脉畸形等混合畸形。
静脉畸形临床表现不一,从独立的皮肤静脉扩张,或局部海绵状肿块,到累及多组织和器官的混合型。出生时即存在,大部分可以被发现,少部分在幼年或青少年时才被发现。头、颈、颌面为好发部位,四肢、躯干次之。其生长速度与身体生长基本同步,不会自行退化,发病无性别差异。覆盖在静脉畸形上的皮肤可以正常, 如累及皮肤真皮层则表现为蓝色或深蓝色;毛细血管静脉畸形的皮肤为深红色或紫色;淋巴静脉畸形混合型表现为皮肤淋巴小滤泡(常伴有过度角化)。局部为柔软、压缩性、无搏动的包块。包块体积大小可随体位改变或静脉回流快慢而发生变化。如静脉畸形在面颈部者,在低头、屏气或压迫颈浅静脉时充盈增大;小儿表现为哭闹或用力挣扎时膨大;病灶位于四肢者,肢体抬高时病灶缩小,低垂或上止血带时则充盈增大。有时可触及瘤体内有颗粒状静脉石。静脉血栓形成,表现为反复的局部疼痛和触痛, 也可因血液淤滞于扩张静脉腔内造成消耗性凝血病。瘤体逐渐生长增大后,可引起沉重感和隐痛。位于眼睑、口唇、舌、口底、咽壁等部位的瘤体,常影响外观,并可引起相应的视力、吞咽、语音、呼吸等功能障碍;侵及关节腔可引起局部酸痛、屈伸异常。静脉畸形也可只发生于肌肉而不侵入皮肤,如常见的咬肌内静脉畸形。皮下静脉畸形可影响邻近的骨骼变化,在面部多表现为骨骼变形及肥大,而在四肢者多表现为骨骼脱钙和萎缩。淋巴静脉畸形多表现为肥大和变形。
2.2 诊断和辅助检查
由病史及详细的体格检查可以确诊大部分静脉畸形患者,但对于分布不明确的病灶,或为了下一步治疗提供治疗依据,可进行下列检查。①瘤体穿刺:从瘤体中央处穿刺,很容易抽到回血;但是,也无法完全排除非血管而血供十分丰富的疾病产生的包块。②X 线平片:可用于确定瘤体范围及骨质的变化;可确认静脉畸形腔内钙化灶及静脉石。③B 超:病灶表现为明显的液性暗区。该检查主要应用于硬化治疗中的穿刺引导,有助于更加准确穿刺至血窦,特别是深部病灶,或多次治疗后残余的分散血窦。④MRI:由于静脉畸形内有丰富的血液及流动性,MRI加权下能清楚显示静脉畸形的范围, 以及与周围组织紧密的关系,应作为首选的检查项目;同时进行血管增强,可区分是否存在其他非血流液体(如淋巴液等)。其典型影像学特征为在T1 加权像为等信号或低信号, 增强时可见不均匀的强化;T2 加权像表现为明显的高信号,抑脂像更能清晰显示病灶。⑤瘤体造影:有经手背或足背浅静脉穿刺的肢体顺行静脉造影和瘤体直接穿刺造影两种静脉造影方法。顺行静脉造影适合于四肢部位的静脉畸形, 尤其针对于广泛多发性的病例。静脉畸形的静脉造影特征为造影剂进入并潴留在与静脉沟通的异常血窦组织内,后者分隔为多腔,单或多发,形态各异。瘤体与主干静脉之间常有数条引流静脉。但如瘤体过大或瘤体与静脉间的交通过细, 顺行造影常不能充分显示整个瘤体,或造影剂不能进入瘤体使之不显影,此时应选用瘤体直接穿刺的造影法。直接穿刺方法,可确定穿刺的瘤腔大小, 特别可以确认瘤体回流静脉血管与正常主干静脉的关系。另外,若瘤腔间交通不畅,需多点穿刺造影,才能较真实反映病灶情况。⑥选择性动脉造影:可显示瘤体的营养和回流血管,对是否存在动静脉瘘有帮助。因是创伤性检查,需酌情考虑。
2.3 治疗
2.3.1 治疗方法及适应证
静脉畸形可累及任何部位, 但以头颈部最为好发,可导致明显的外观畸形和器官移位;巨大的病灶还可导致面部骨骼发育异常。在肢体和躯干静脉畸形,尤其是弥散型病变中,因血流缓慢淤滞会出现病灶内血栓形成,可引起不同程度的疼痛,甚至功能障碍。因此,对于头面部和伴有疼痛的肢体病灶,应尽早治疗,控制病情进一步发展。
治疗静脉畸形的主要方法是血管内硬化治疗,这是多年发展后的共识。当然,还有其他的非手术和手术方法,可根据畸形的范围、界限、部位单独或联合使用。非手术治疗包括血管内硬化治疗、激光治疗、铜针留置术、电化学及患肢压迫治疗等。手术切除治疗包括单纯手术切除、硬化术后手术切除、热凝及其他治疗后手术,以及相关的修复重建手术。
2.3.2 治疗方法的选择
2.3.2.1 血管内硬化治疗
目前国际主流的治疗方法为血管内硬化治疗(Intravascular sclerotherapy),即通过无水乙醇、博来霉素(平阳霉素)、泡沫硬化剂(聚多卡醇、聚桂醇、十四烷基硫酸钠)或鱼肝油酸钠等硬化剂破坏血管内皮细胞,造成病灶血管的纤维化闭塞和体积的萎缩,实现外观和功能的康复,复发概率较小。但是,广泛而弥散的病灶需多次治疗,而且效果相对较差。
治疗时,从病灶穿刺,回抽见缓慢静脉血流出,治疗在全麻、病灶内局麻或神经阻滞麻醉下进行,要切实保证必要的止痛才可治疗。如非在DSA 下操作,则穿刺点至少两点以上,明确互相流通,才能再进行硬化剂注射, 减少进入动脉或动脉穿支的可能性,以免引发严重并发症。单次治疗,无水乙醇剂量不超过0.2 mL/Kg,聚桂醇单次剂量不超过8 mL,博来霉素总剂量不超过300~400 mg。当瘤体侵及眼眶球后、颈部等很多危险区域时,建议在DSA 下评估治疗的安全性,再行血管内治疗。在多次治疗后因血窦腔缩小致穿刺难度明显增加时,需在B 超引导下精准定位残留病灶,以提高疗效。治疗完毕,穿刺点压迫片刻,局部制动3 d,患部应高于心脏位置以便肿胀消退。
治疗伴随相关并发症,如深部瘤体侵犯肌肉,治疗后可产生短暂性肌肉痛,并较僵硬,1 个月后逐渐恢复正常;如有神经穿过瘤体导致的损伤多为可逆性损伤;如采用平阳霉素治疗可出现过敏性休克,并常在多次治疗后出现;如误入动脉系统可能导致灾难性的组织器官,甚至肢体坏死,即使没有注入动脉内,治疗也可能导致水泡和皮肤坏死。另有血管内治疗后出现心肺危象而导致死亡的报道,其机理不清,需随时警惕。减缓静脉回流是提高疗效,减少并发症的重要措施。
2.3.2.2 手术治疗
静脉畸形病灶内有丰富的腔窦及周围血管,除了部分界限较清楚的局限性异常扩张病灶外, 绝大多数是弥漫且与正常组织界限不清的病灶, 难以手术切除,并对局部组织的功能和形态影响较大,创伤大、出血控制难、复发快、功能和外观影响大。因此,手术不是静脉畸形的首选治疗方法。
手术治疗仅在必要的情况下才使用, 如弥散型的静脉畸形对硬化治疗反应差, 需要手术修复达到外观改善,此类型的巨唇、眼睑臃肿、面部软组织萎缩等都是手术治疗的适应证;对血管内治疗后残留病灶的外观改善、功能重建(如继发跟腱短缩延长等)也需要手术辅助;头面部大范围静脉畸形经过多次过度硬化治疗后,可能导致局部凹陷畸形,或因并发症导致凹陷甚至瘢痕等, 可应用吻合血管或游离的筋膜瓣或筋膜脂肪瓣充填;合并骨骼畸形的患者可以通过截骨和轮廓整形获得良好的美容效果。对于疑难静脉畸形病例,如涉及眼眶内、颅内外沟通或肢体骨骼畸形的VM, 手术也可能是很重要的配合手段之一,成为静脉畸形多学科、序列化、美容性治疗计划的一部分。手术原则应在保存基本功能的情况下, 仔细分离, 保护神经血管肌腱等重要组织结构,进行适当的切除。
2.3.2.3 激光治疗
皮肤或黏膜的浅表静脉畸形可采用激光治疗,分为非侵入性激光治疗和侵入性激光凝固技术,后者又可分为血管腔内激光凝固技术和组织内激光凝固技术。激光治疗体表静脉畸形的理论基础是选择性光热作用, 激光光能被还原型血红蛋白选择性吸收,引起血管腔内血栓形成、血管壁损伤、血管闭合。长脉冲1 064 nm Nd:YAG 激光是治疗浅表静脉畸形的首选,其穿透深度为4~6 mm,能有效作用于浅表病灶。脉宽选择在7~8 ms 时,不会出现明显的血管爆裂和紫癜,能观察到病灶即刻凝固收缩,治疗后局部组织不出现萎缩, 其主要不良反应为色沉、水泡和组织坏死。优化能量、脉宽和脉冲数量的组合,能有效避免上述不良反应,具有较高的安全性。
3 动静脉畸形
3.1 临床表现
动静脉畸形(Arteriovenous malformation,AVM)是一种高流量的先天性血管畸形,由扩张的动脉和静脉组成, 异常的动静脉之间缺乏正常毛细血管床。AVM 发生率低,无性别差异。40%~60%的患者出生时即发现, 易被误诊为毛细血管畸形或血管瘤。头颈部相对好发,其次为四肢、躯干和内脏。病灶局部表现为皮肤红斑,皮温高,可触及搏动或震颤。局部可出现疼痛、溃疡或反复出血,严重者因长期血流动力学异常可致心力衰竭。AVM 还引起外观畸形,重要组织器官受压及功能损害等。AVM 按照疾病进展的严重程度分为4 期(表4)。
3.2 诊断
绝大多数AVM 可通过临床表现明确诊断。和血管瘤不同,AVM 病灶在婴儿期无明显增生变大的病程。AVM 的高流量特征可使之与毛细血管畸形、静脉畸形或淋巴管畸形等区别。
3.3 辅助检查
通过临床表现如不能明确诊断, 可利用影像学检查辅助。彩色多普勒可检测AVM 的高流量特征。MRI 有利于明确病灶范围。DSA 是AVM 诊断的金标准,治疗前需进行DSA 检查,为治疗方案的选择提供指导。如果病灶累及骨骼,则需行CTA 检查。除了疑似恶性肿瘤不能明确诊断的病例, 活检通常不必要,且活检创伤可能引起病灶出血和病情加重。
3.4 治疗
AVM 治疗困难,复发率高。病灶供血动脉结扎或供血动脉近端栓塞,因瘘口未充分处理,通常会加重病情,且不利于后期治疗,这种有害无益的治疗方式应予废弃。AVM 治疗方式包括常规介入栓塞、无水乙醇介入治疗、外科手术、联合治疗等。目前尚无成熟的药物治疗方式。
3.4.1 常规介入栓塞
常规的介入栓塞剂可以是液体, 如NBCA 或Onyx 等, 也可以是固体, 如明胶海绵粉、PVA(Polyvinyl alcohol)及弹簧圈等。因常规栓塞剂不能破坏血管内皮细胞,无法去除AVM 病灶,绝大多数患者最终都会复发,但该治疗可减少术中出血,目前的常规介入栓塞主要用于手术前准备。
3.4.2 无水乙醇介入栓塞治疗
无水乙醇可破坏血管内皮细胞, 是一种效果彻底的治疗方法。但误栓可引起周围正常组织坏死、重要器官功能丧失(如失明), 甚至是心肺衰竭死亡。该治疗必须由经验丰富的专科医师实施,以尽可能减少严重并发症的发生。对于很多颅外AVM,如果能够有效控制并发症率, 无水乙醇介入是颅外AVM 首选的有治愈潜力和高度选择性的一线治疗方法。
3.4.3 外科手术
外科手术在无水乙醇介入栓塞出现以前, 一直是AVM 治疗的主要方法。彻底清除病灶是手术治疗的理想目标。病灶切除后的缺损, 不建议直接植皮,可予局部皮瓣、扩张皮瓣或游离皮瓣修复。彻底的手术切除可实现病灶区域的长期稳定,不再复发,而不完全的切除通常与后期的复发有关。严重的、范围过大和已经导致严重并发症如出血、疼痛或坏死的肢体动静脉畸形,最终需要截肢。无水乙醇介入方法的出现虽然改变了AVM 的治疗模式, 但仍无法完全取代外科手术。
对于无水乙醇介入治疗潜在风险较大的患者,或因病灶难以通过介入途径实现有效治疗, 以及畏惧严重并发症的病例,手术仍是必要的治疗方式。另外,无水乙醇介入栓塞治疗的并发症(如误栓所致的组织坏死),亦需依靠整形手术以改善外观。
3.4.4 联合治疗
无水乙醇介入栓塞技术和外科手术技术,包括器官重建技术、显微外科技术、颌面外科技术、美容外科技术等均熟练掌握的联合治疗团队可有效实现针对同一患者应用多学科技术的联合应用, 实现患者在疗效和安全性方面的利益最大化。
4淋巴管畸形
淋巴管畸形(Lymphatic malformation,LM),以往称为淋巴管瘤,是常见的一种先天性脉管畸形疾病。根据淋巴管囊腔的大小,可将LM 分为巨囊型、微囊型和混合型等三中类型。巨囊型LM 由1 个或多个体积≥2 cm3 的囊腔构成(即以往所称的囊肿型或囊性水瘤),而微囊型LM 则由多个体积<2 cm3 的囊腔构成(即以往的毛细管型和海绵型),二者兼而有之的则称为混合型LM。LM 发病率为1/4 000-1/2000,尚未发现有性别和种族差异。该病多在2 岁前发病,约50%患者出生时即发现罹患此病。LM 可发生在具有淋巴管网的任何身体部位,约75%病变发生在头、颈部,其次为腋窝、纵膈及四肢。
4.1 淋巴管畸形的组织病理和发病机制
LM 的发病机制尚不清楚, 一般认为其病变内皮细胞均可能来源于脉管系统发育的早期。在胚胎期,静脉丛中的中胚层首先形成原始淋巴囊,淋巴囊再逐渐形成有功能的毛细淋巴管, 毛细淋巴管相互吻合成网, 逐渐汇集成一系列由小到大的各级淋巴管。在此过程中, 由于某种原因可使淋巴管系统紊乱, 造成淋巴管非恶性的异常生长和扩张, 即形成LM 组织。其病理学特点:LM 内皮细胞组成的壁薄、形态不规则及大小各异的淋巴管腔内充满淋巴液,周围则有大量的成纤维细胞、白细胞、脂肪细胞和肌细胞等。但是,在LM 的整个病理过程中,无LM 内皮细胞数量的增加,且其形态和功能也表现正常,仅淋巴管管腔直径发生变化。研究发现,淋巴管畸形伴有其他血管畸形或过度发育的综合征中存在体细胞PIK3CA 突变。淋巴管畸形、CLOVES 综合征、FAVA及KT 综合征也称为PIK3CA 相关过度发育疾病谱。
4.2 临床表现及诊断
淋巴管畸形的临床症状多比较典型,结合超声、诊断性穿刺、CT 及磁共振检查, 必要时依据情况辅以活检,基本可以确诊。
淋巴管畸形可以发生在全身任何部位, 其中以主要淋巴系统所在区域最为常见, 因此颈部及腋下发病率最高,腹股沟、纵膈、腹膜后次之,躯干及四肢最低。巨囊型淋巴管畸形通常由不止一个囊腔组成,囊腔之间可相通或不相通。囊腔中含有水样的透明液体,有波动感,有时不透光或呈琥珀色。而微囊型淋巴管畸形的病灶相对较实质性。淋巴管畸形的临床表现受病变的类型、范围和深度的影响而差异很大。有些表现为皮肤黏膜上充满液体的小泡,有些则表现为巨大的肿物。
结合病史和体检怀疑为淋巴管畸形时, 应常规先行超声检查,明确瘤体的部位、性质、大小及与周围组织的关系,为手术或药物注射治疗提供依据,并可用于监测预后情况。MRI(血管增强)检查可提供比较可靠的客观图像并区分淋巴管和血管。深入了解瘤体的位置及与周围组织的关系, 对于颈腋部较复杂位置以及腹盆腔较深位置的瘤体, 在超声不能明确诊断时可用于鉴别诊断,也可辅助诊断性穿刺,若穿刺抽出淡黄色清亮淋巴液即可诊断为淋巴管畸形, 若抽出陈旧性血液结合细胞学检查可诊断为淋巴管瘤伴出血。
4.3治疗
LM 被认为是淋巴系统的良性病变,生长缓慢、很少自然消退。但在遭受创伤、感染及发生囊内出血或不适当治疗后,常突然增大。若LM 生长在特殊部位,则可能导致毁容、畸形、压迫重要器官引起功能障碍,造成长期后遗症,甚至危及患者生命。故对该病需采取积极恰当的干预措施。
以往认为手术是LM 最主要的治疗手段, 但目前LM 的治疗方法多种多样,包括手术切除、激光治疗、硬化剂注射(如注射博来霉素、强力霉素、无水乙醇及OK-432)等。但尚无一种方法可以治疗所有类型的LM。硬化治疗适用于巨囊型和混合型淋巴管畸形,其疗效令人满意;但对微囊型淋巴管畸形则疗效较差。相对于手术治疗,硬化治疗有以下优点:①创伤小,不易损伤重要神经、血管、腺体、肌肉等组织结构;②巨囊型效果良好、治愈率高、不易复发;③操作简便,比较安全;④外形恢复良好,无明显瘢痕。进行硬化剂注射治疗时, 应根据病灶特点, 进行分部位、多次囊腔内注射治疗,避免损伤重要神经、腺体等。一般应抽尽或接近抽尽每个囊腔中的淋巴液,再注入合适剂量与浓度的硬化剂。对于侵犯口底、咽旁、气道周围的病例,为避免治疗后肿胀引起的气道阻塞,治疗前需争取行气管切开术。若气管切开区域有病灶,可先行治疗。目前常用的硬化剂有博来霉素(平阳霉素)、溶血性链球菌制剂OK-432(沙培林)、强力霉素、无水乙醇和泡沫硬化剂等。
手术治疗是过去最主要的, 甚至是唯一的治疗手段,但随着硬化治疗的开展和经验的积累,目前不主张毫无选择地对任何类型的LM 都进行手术切除,只有极少数病例需要在婴幼儿期行手术切除。尽管LM 呈缓慢增大倾向,但并不会侵犯周围组织。局限性大囊型病变可以手术完全切除, 但弥漫性微囊型病变完全切除很困难。目前认可的手术指征:①病灶较小,位置较好,可完全切除;②有症状的微囊型淋巴管畸形;③硬化治疗后仍有症状的巨囊型及混合型淋巴管畸形;④有危及生命的并发症;⑤对外观影响较大。手术切除淋巴管畸形首先需考虑到其良性疾病的性质,保证重要结构的保留。考虑到病灶区重要神经血管的保护, 大多数情况下次全切除或部分切除更为恰当。残留的病灶可通过注射硬化剂进一步治疗。对于头面部淋巴管畸形,巨囊型的舌骨下和舌骨上LM 完全或次全切除的可能性较大, 对于双侧较大病灶并伴有上呼吸道压迫的患者,手术切除应为首选治疗方法。手术必须将单侧或双侧颈部功能性结构解剖清楚,如病灶过大可分期手术。弥漫型的微囊型淋巴管畸形对手术亦是很大的挑战,其病灶浸润周围组织及器官,使解剖结构不清楚,难以分辨其边界。双侧舌骨上伴有上呼吸道压迫的LM只能行部分手术切除, 术后应注意水肿引起的上呼吸道压迫症状。气管切开和放置胃管对于预防压迫发生很重要。联合应用激光、硬化等方法,对于大面积的病灶也很关键。
药物治疗是目前淋巴管畸形治疗研究的热点。目前,最广泛被使用的药物为西罗莫司。西罗莫司又名雷帕霉素,是mTOR (Mammalian target of rapamycin)受体抑制剂。mTOR 在细胞合成分解代谢,细胞运动, 细胞生长及血管生成方面均起到关键的作用。mTOR 通路可以调节做为淋巴管生成和血管生成的关键调节因子VEGF 来影响脉管的生成。根据目前的病例报道及临床实验结果, 建议对于严重的淋巴管畸形, 如GLA、KLA、Gorham-Stout Syndrome及弥漫型淋巴管畸形,可在患者知情同意下使用。初始剂量为0.1 mg/Kg·d 或0.8 mg/m2·d, 后续调整剂量使血药浓度维持在10~15 ng/mL, 对于婴幼儿患者需同时口服复方新诺明,以预防肺部感染。
原文来自:组织工程与重建外科杂志2019 年10 月第15 卷第5 期 (如有侵权,请联系及时删除)
![时事焦点-[血管瘤和血管瘤的治疗]血管瘤和脉管畸形的诊断及治疗指南2019版 时事焦点-[血管瘤和血管瘤的治疗]血管瘤和脉管畸形的诊断及治疗指南2019版](http://51ac.top/zb_users/theme/Blogs/image/logo.png)

发表评论